The Lancet
Tratamiento sin quimioterapia para el cáncer de mama temprano HER2+
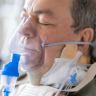
Un enfoque basado en el uso de los anticuerpos trastuzumab y pertuzumab, con un seguimiento por PET, detiene la progresión de este subtipo tumoral en estadios I-IIIA en un tercio de las mujeres desde los 18 años.
El cáncer de mama HER2+ se ha correlacionado con un alto riesgo de recurrencia y mal pronóstico, sin embargo, la introducción de terapias dirigidas a HER2 ha mejorado la supervivencia y ha abierto una puerta a reducir la quimioterapia en subgrupos seleccionados.
El grupo de investigación del MD. José Manuel Pérez García del Centro Internacional de Cáncer de Mama (IBCC) en Barcelona – España, diseñó el estudio PHERGain para evaluar la viabilidad, seguridad y eficacia de un tratamiento sin quimioterapia basado en el bloqueo dual de HER2 con trastuzumab y pertuzumab en pacientes con cáncer de mama temprano HER2+.
PHERGain fue un ensayo de fase 2, aleatorizado y abierto, que se llevó a cabo en 45 hospitales de siete países europeos. Participaron 356 mujeres (desde los 18 años) con el tumor operable, invasivo en estadio I-IIIA, HER2+ y con al menos una lesión evaluable por PET con F18-fluorodesoxiglucosa. Se asignaron aleatoriamente, en una proporción de 1:4, ya sea al grupo A (n= 71), donde recibieron el esquema TCHP: docetaxel (75 mg/m2, intravenoso), carboplatino (AUC 6 mg/ml por min, intravenoso), trastuzumab (dosis fija de 600 mg, subcutánea) y pertuzumab (dosis de carga de 840 mg seguida de dosis de mantenimiento de 420 mg, intravenoso), o grupo B (n= 285), donde les suministraron trastuzumab y pertuzumab con o sin terapia endocrina, cada 3 semanas. La aleatorización se estratificó según el estado del receptor hormonal. Se realizó la PET al inicio y después de dos ciclos de tratamiento y según los resultados se dio continuidad. Aquellas que no respondieron a la terapia con anticuerpos fueron cambiadas al esquema TCHP.
Los criterios de valoración principales fueron la respuesta patológica completa en las pacientes del grupo B que respondieron a la PET después de dos ciclos de tratamiento y la supervivencia libre de enfermedad invasiva a 3 años. El estudio sigue en curso.
Con una mediana de seguimiento de 43,3 meses, 63 (89%) y 267 (94%) pacientes fueron sometidas a cirugía en los grupos A y B, respectivamente. En el grupo B, la tasa de supervivencia libre de enfermedad invasiva a 3 años fue del 94,8% (IC 95%; P= 0,001). El grupo A presentó mayores eventos adversos relacionados con el tratamiento (grado ≥3, 62% frente a 33%) y graves (28 % frente a 14 %). Las participantes del grupo B que tuvieron una buena respuesta al tratamiento presentaron la incidencia más baja de estos eventos.
Estos resultados preliminares muestran que, una estrategia adaptada a la respuesta patológica completa basada en PET se asocia con una excelente supervivencia libre de enfermedad invasiva a 3 años en pacientes con cáncer de mama temprano HER2+. Se determinó que un tercio de las participantes podían omitir la quimioterapia de forma segura.
Temas Relacionados