Clasificador de células: velocidad y precisión
La clasificación de células a través de diferentes técnicas, unas más avanzadas que otras, permite a los científicos identificar y catalogar células individuales en función de sus características específicas para estudiarlas con más detalle, evaluar cómo cada una de ellas puede reaccionar a un nuevo fármaco o realizar otros estudios.
Los métodos que separan físicamente las células de interés en base a características medibles tienen numerosos usos en aplicaciones clínicas y de investigación, incluyendo terapias celulares. La microfluídica, los filtros y la centrifugación se utilizan para identificar y separar físicamente las células de una población heterogénea según características intrínsecas como el tamaño, la forma y la deformabilidad. También se pueden ordenar en función de señales de las sondas extrínsecas.
La clasificación de células activadas por fluorescencia (FACS) es el medio más popular para separar una población en subconjuntos de acuerdo con la cantidad total de biomarcadores que expresa cada unidad. Estos biomarcadores generalmente se detectan con anticuerpos marcados con fluorocromo. Nuevas investigaciones informan sobre un atractivo sistema que clasifica las células según la apariencia de los biomarcadores (es decir, sus propiedades morfológicas), no solo la cantidad de cada biomarcador, a velocidades de hasta 15.000 células por segundo.
El instrumento prototipo es una adaptación del clasificador de células BD FACSMelody (BD Biosciences), que se considera el caballo de batalla de FACS. Aunque tiene unos pocos canales de fluorescencia (los sistemas FACS tienen muchos más), clasifica las células según el patrón espacial de fluorescencia (por el contrario, FACS convencional mide solo la señal de fluorescencia total). El sistema se basa en imágenes rápidas de fluorescencia que utilizan emisión etiquetada por radiofrecuencia y electrónica especializada de procesamiento y clasificación de señales de baja latencia, un inteligente enfoque que proporciona información espacial para cada señal. La sensibilidad del prototipo coincide con la FACS convencional, pero no utiliza cámaras lentas y costosas, un avance que es el más reciente de una serie de instrumentos que permiten la clasificación física según fenotipos morfológicos y de localización. Este sistema es más rápido y tiene más contenedores de clasificación que los predecesores.
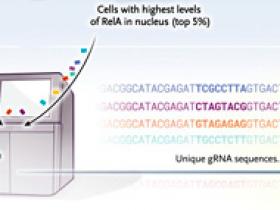
Cuando se probó por primera vez utilizando células que expresaban proteínas fluorescentes dirigidas a orgánulos específicos (figura 1), se pudo detectar cambios en la localización inducidos por varios fármacos. Luego se examinaron los efectos que resultaron de la ablación de loci genéticos específicos en todo el genoma humano (usando la enzima Cas9 y el ARN guía) para identificar los reguladores de la translocación de una proteína marcada con fluorescencia (RelA) en el núcleo cuando se estimula la célula por el factor de necrosis tumoral α (TNF-α). RelA es un miembro de la familia de factores de transcripción NF-κB, implicados en una amplia gama de enfermedades, en particular la disfunción inmunitaria y el cáncer. Por lo general, se ubica en el citoplasma de las células; y cuando es activado por varios estresores ambientales se traslada al núcleo.
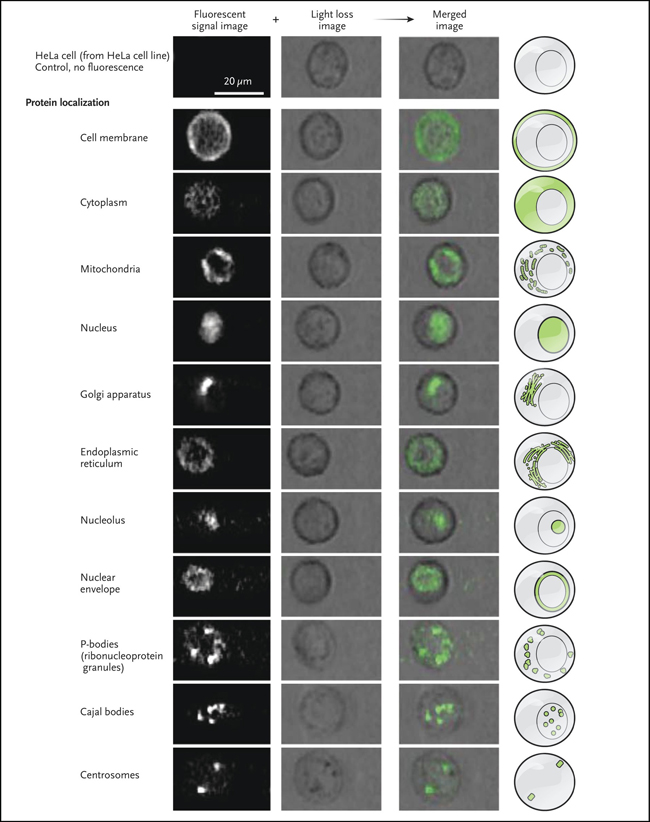
Figura 1: fenotipos de localización basados en imágenes detectables en células en suspensión.
El clasificador separó físicamente las células que tenían expresión nuclear de RelA después de 9 horas de tiempo de ejecución a una velocidad de clasificación de 14 millones de células por hora. Se han podido identificar loci específicos, cuya ablación bloquea la translocación nuclear de RelA. Esto se ha hecho mediante la secuenciación de ARN guía únicos que servían como códigos de barras en las células afectadas (figura 2). En general, parece que este sistema puede clasificar adecuadamente las células sobre la base de características morfológicas complejas preespecificadas.
Las tecnologías de clasificación de células basadas en imágenes tienen innumerables aplicaciones. Primero, los reactivos genéticos con código de barras que están presentes en las poblaciones de células ordenadas por imágenes se pueden secuenciar, lo que permite una poderosa eliminación de todo el genoma o pantallas de sobreexpresión. Esta aplicación extiende la cantidad de fenotipos que se pueden examinar para identificar los genes que subyacen a los fenotipos celulares relacionados con enfermedades, un desarrollo que podría se capaz de descubrir potenciales objetivos terapéuticos (figura 2).
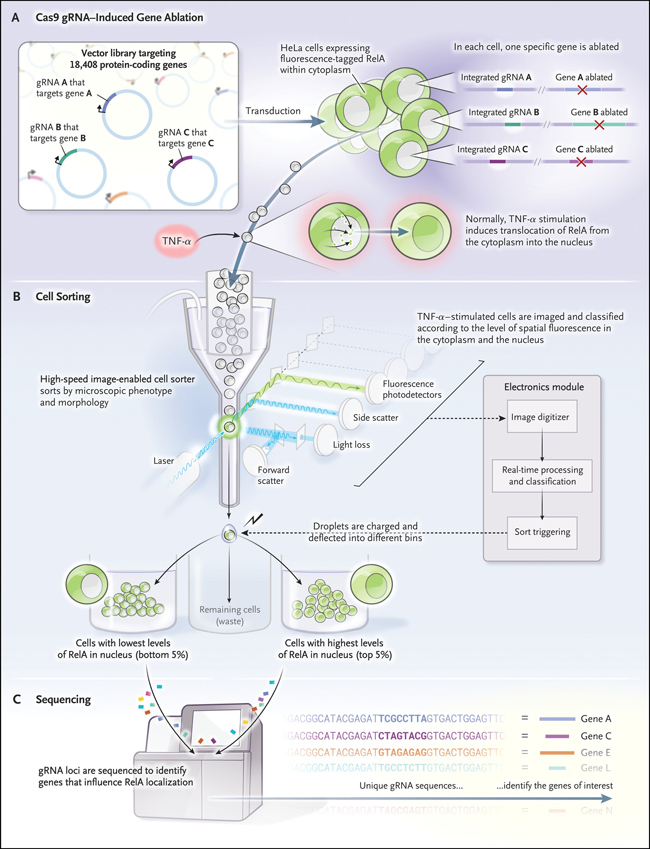
Figura 2: detección de perturbaciones genéticas en el genoma.
Existen otros enfoques para el cribado en base a imágenes que son muy adecuados para experimentos específicos. Los basados en el microscopio suelen ser más lentos que los sistemas de flujo, pero permiten la detección de características morfológicas que solo son perceptibles a mayor resolución o en células que están adheridas y esparcidas sobre una superficie de vidrio. La detección con microscopía implica la ablación selectiva de células o la iluminación de células, un proceso al que sigue la disociación y la clasificación. Alternativamente, los enfoques basados en microscopios son capaces de detectar perturbaciones genéticas en cada célula fotografiada in situ, permitiendo volver a analizar las imágenes capturadas para detectar otros fenotipos y realizar mediciones precisas y continuas de fenotipos para cada perturbación genética probada (en lugar de clasificar las tecnologías que solo cuentan la frecuencia con la que se encuentra una célula con una característica particular en cada contenedor de clasificación).
La clasificación celular basada en imágenes se puede utilizar para explorar la relación entre los fenotipos de células visibles ordenados y otras características. Las subpoblaciones clasificadas según características morfológicas podrían analizarse posteriormente en cuanto a su genoma, transcriptoma, epigenoma, proteoma o propiedades morfológicas adicionales. Además, las poblaciones se pueden comparar según la respuesta a perturbaciones como los tratamientos farmacológicos.
Finalmente, la clasificación de células basada en imágenes lograría usarse simplemente para obtener muestras de células que no pueden purificarse en la misma medida con FACS convencional, ya sea para investigación o uso clínico. Por ejemplo, una aplicación podría ser purificar, enriquecer y hacer crecer subtipos de células, como células tumorales circulantes, ex vivo, para diagnóstico y para probar varios medicamentos para guiar las opciones terapéuticas. En otra potencial aplicación, los productos sanguíneos podrían purificarse para eliminar las células dañadas que se identifican sobre la base de las características morfológicas. Las células madre con propiedades favorables se clasificarían según el potencial de diferenciación o por objetivos terapéuticos definidos.
Por supuesto, usos posteriores de células clasificadas requieren que estén libres de fijadores o marcadores tóxicos, que son necesarios para la detección de muchos fenotipos. Afortunadamente, los avances en el aprendizaje están comenzando a mostrar que las imágenes de campo brillante sin etiquetas son prometedoras para la identificación de fenotipos complejos e inesperados que anteriormente se pensaba que requerían marcadores específicos; se podría entrenar una computadora para que reconozca células de un estado de enfermedad dado (por ejemplo, leucemia) o para convertir imágenes sin etiquetar en imágenes fluorescentes artificiales. Las tecnologías de clasificación requieren la clasificación de cada célula en tiempo real, y la clasificación de células con fenotipos complejos requiere aprendizaje automático. Por lo tanto, queda por ver si las células con complejos fenotipos podrían clasificarse con éxito. Sin embargo, estos avances apuntan a un futuro en el que las subpoblaciones de células de precisión se purifiquen rápidamente y así aprovecharlas debidamente.
Fuente bibliográfica
A New Image for Cell Sorting
A. Filby and A.E. Carpenter
Innovation, Methodology, and Application Research Theme, Faculty of Medical Sciences, Newcastle University, Newcastle upon Tyne, United Kingdom (A.F.); and the Broad Institute of MIT and Harvard, Cambridge, MA (A.E.C.).
N Engl J Med 2022; 386:1755-1758