Terapia CAR-T para la fibrosis cardíaca
Los linfocitos T con receptor de antígeno quimérico autólogo, diseñados para unirse y destruir células que expresan un antígeno específico, son eficaces en el tratamiento de ciertos tipos de cáncer. Ahora, un estudio reciente en un modelo de ratón muestra que las células CAR-T pueden generarse in vivo y controlar la fibrosis.
La fibrosis, o cicatrización, es una respuesta a la lesión tisular que se da en todo el cuerpo humano. Más del 40 % de todas las muertes en el mundo industrializado son atribuibles a la cicatrización del corazón, el hígado, los pulmones, los riñones, la médula ósea o la piel, entre otros tejidos. Los principales avances han mejorado su comprensión, en particular, la identificación de las células fibrogénicas dentro de cada tejido. Un paradigma es que las células mesenquimatosas perivasculares residentes (pericitos y fibroblastos) que albergan características compartidas y únicas en los tejidos, se transforman, al activarse a través de una lesión tisular, en células fibrogénicas contráctiles (miofibroblastos) que secretan moléculas "cicatriciales", principalmente colágenos intersticiales y glicoproteínas especializadas, para crear una densa red que interfiere con la función del órgano.
A pesar de los efectos adversos de la cicatrización en la salud humana, no existen terapias aprobadas que la revierta. Sin embargo, recientemente Joel G. Rurik y colaboradores han descrito una estrategia para eliminar las células productoras de cicatrices del corazón lesionado, lo que es motivo de optimismo. Las investigaciones se han basado en estudios previos que habían demostrado el potencial de las células T con receptores quiméricos de antígenos (CAR-T, desarrolladas originalmente para suprimir células cancerosas) para eliminar células fibrogénicas no malignas de corazón e hígado de ratón, respectivamente. Las unidades CAR-T están diseñadas para concentrarse en receptores específicos en las células objetivo y destruirlas. Los estudios están dirigidos al péptido de activación de fibroblastos (FAP) de la superficie celular de los fibroblastos cardíacos activados, que en el corazón es exclusivo de este tipo de células. El estudio involucró a las células CAR T que se dirigen al receptor del activador del plasminógeno de tipo uroquinasa, que se expresa mediante miofibroblastos hepáticos senescentes fibrogénicos que se derivan de las células estrelladas hepáticas residentes (pericitos) (figura 1).
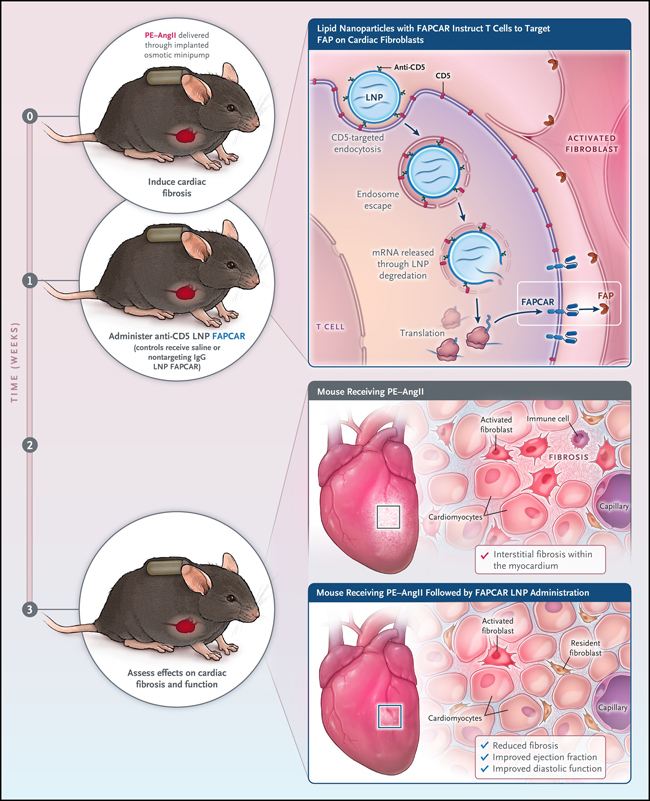
Figura 1: generación de células CAR-T para tratar la fibrosis cardíaca.
Novedoso método para crear células T con receptor de antígeno quimérico (CAR) especializadas que se programan in vivo para atacar y destruir los fibroblastos cardíacos. Las nanopartículas de lípidos FAPCAR contienen ARN mensajero (ARNm) que codifica un CAR que se une a la proteína de activación de fibroblastos (FAP) en los fibroblastos cardíacos y los elimina. Se administraron nanopartículas de lípidos FAPCAR a ratones con fibrosis cardíaca inducida por la administración de fenilefrina y angiotensina II (PE-AngII) durante 7 días. Dos semanas más tarde, con la administración continua de PE-AngII, los ratones sin tratamiento con FAPCAR tenían fibrosis intersticial en el miocardio, mientras que los que recibieron nanopartículas lipídicas de FAPCAR presentaban menos acumulación de fibrosis y mejor función cardíaca (fracción de eyección y función diastólica). En lugar de la inducción ex vivo de la expresión CAR especializada, esta técnica implica la inyección de una nanopartícula lipídica dirigida a los linfocitos T mediante un anticuerpo que se une al receptor CD5 en las células T. Después de la captación en el endosoma de las células T, el ARNm que codifica CAR se traduce en proteína y se dirige a la célula T para que se una a FAP en la superficie celular de los fibroblastos cardíacos.
Informes anteriores establecieron que la enfermedad fibrótica en modelos de ratón podría tratarse con el uso de células CAR-T. Sin embargo, la generación de éstas implica la extracción de linfocitos y la transducción ex vivo con un vector retroviral de ADN que codificaba un CAR que instruye a las células para encontrar y eliminar su objetivo. A continuación, las unidades transfectadas se reintrodujeron en el ratón. Este complicado método podría dificultar su implementación. Pero en este estudio se exploró la tecnología de nanopartículas lipídicas que contienen secuencias de ARN mensajero (ARNm), cuya seguridad y escalabilidad se han establecido mediante la utilización en vacunas de ARNm contra Covid-19, para producir células CAR-T para el tratamiento de la fibrosis. Los investigadores generaron nanopartículas lipídicas que tienen una señal (anti-CD5) en su superficie que las dirige a las células T in vivo, y dentro de cada partícula hay un ARNm que codifica un CAR diseñado para unirse a FAP (el CAR se llama FAPCAR). En la fusión de la nanopartícula lipídica con la célula T, el ARNm ingresa al citoplasma y se traduce en FAPCAR, equipando a las células T con la capacidad de reconocer y unirse al fibroblasto cardíaco activado (porque este expresa FAP en su superficie).
Las nanopartículas lipídicas que contienen el ARNm que codifica FAPCAR, cuando se administraron a ratones con fibrosis cardíaca experimental, se comportaron de manera similar a las células CAR-T dirigidas por FAP fabricadas convencionalmente (es decir, "ex vivo"): una comparación de los estudios realizados al respecto muestra que cada enfoque da como resultado la muerte de las células que expresan FAP in vivo, lo que reduce la fibrosis y mejora la función cardíaca.
Los hallazgos representan un avance por varias razones. Primero, en lugar de depender de un método ex vivo para preparar células T con CAR, el enfoque descrito permitiría que el tratamiento se distribuya como una nanopartícula de lípidos terapéuticos con control de calidad "lista para usar": ARNm que genera la célula T con CAR, producto in vivo, muy parecido a las vacunas actuales de ARNm de Covid-19. Segundo, la expresión del ARNm es transitoria (no hay integración de ácido nucleico en el genoma del huésped), lo que disminuye el riesgo de alteraciones genéticas a largo plazo y permite ajustar la dosis y repetir la administración según sea necesario. Finalmente, la notable seguridad de la tecnología de ARNm de nanopartículas lipídicas se ha establecido a través de su uso en millones de pacientes en todo el mundo.
Sin embargo, estos resultados también plantean preguntas y señalan desafíos. ¿Funcionaría el enfoque cuando la fibrosis es extensa y da como resultado un acceso reducido a las células fibrogénicas (debido a la cicatrización y distorsión del tejido que crea)? La elección del objetivo de la superficie celular para las células CAR-T será fundamental, pudiendo variar entre diferentes órganos y especies; el principal motivo debe restringirse al tejido lesionado donde se concentra la fibrogénesis, para minimizar los efectos en otros tejidos. Identificar el objetivo ideal de la superficie celular en contextos específicos es un desafío. Las células fibrogénicas pueden respaldar la función normal de los órganos y su eliminación interrumpiría la regeneración y reparación de los tejidos, especialmente en el corazón, donde la pérdida completa de la cicatriz provocaría la ruptura cardíaca, y en el hígado, donde las células estrelladas hepáticas también poseen importantes funciones homeostáticas. Finalmente, existe la necesidad de pruebas rigurosas de replicación por parte de laboratorios independientes. No obstante, estas preguntas proporcionan una base para futuras investigaciones de esta forma de "tecnología de misiles guiados" en la eliminación de tipos de células que causan enfermedades en una variedad de condiciones.
Fuente bibliográfica
Fighting Cardiac Fibrosis with CAR T Cells
Scott L. Friedman, M.D.
Division of Liver Diseases, Icahn School of Medicine at Mount Sinai, New York.
N Engl J Med 2022; 386:1576-1578