Proyecciones clínicas de los ARN glicosilados
Los descubrimientos en el ARN no codificante han demostrado que es notablemente diverso en función y forma, lo que podría tener relevancia en el desarrollo de fármacos. Ciertos ARN no codificantes están glicosilados y sialilados, expresándose en la superficie de la membrana plasmática. Además, algunos interactúan con Siglec-15, un inmunosupresor que se activa en células cancerosas humanas y en células mieloides que se infiltran en el tumor.
Los ARN se modifican con diversos grupos químicos, que van desde simples grupos metilo hasta otros más complejos. Estas alteraciones son esenciales para sus diversas funciones como catalizadores, armazones estructurales y reguladores de la expresión génica. Sin embargo, aparte de algunas modificaciones en los ARN de transferencia, no existía evidencia de ARN glicosilado.
En un descubrimiento que se predice en partes iguales (para la existencia de una biomolécula glicosilada) y, sin embargo, en un cambio de paradigma (para el ARN), Ryan Flynn y colegas informaron que el ARN también puede glicosilarse y, además, sializarse para formar glicoARN, que se localizan en la superficie celular. El etiquetado metabólico de las células vivas reveló la incorporación del azúcar manosa en un grupo de pequeños ARN no codificantes que incluyen Y ARN, que tienen un papel en la replicación del ADN y forman un complejo ARN-proteína que es el objetivo de anticuerpos en pacientes con lupus eritematoso sistémico y síndrome de Sjögren.
Hasta ahora, la modificación con azúcares se ha asociado principalmente a lípidos y proteínas que se secretan o están en la superficie celular. Las modificaciones del azúcar se introducen a través de una serie de eventos altamente coordinados, y cada paso de glicosilación ocurre en orgánulos separados a través de los cuales transita la carga, comenzando en el retículo endoplásmico y terminando con vesículas secretoras que contienen la carga glicosilada que se fusiona en la superficie celular (figura 1A). Las diferentes etapas de la glicosilación ocurren con una topología de membrana muy específica y sirven como mecanismos de control de calidad durante todo el proceso de secreción. La glicosilación guía el plegado adecuado de la carga, asegura su tráfico y, a veces, actúa como una capa protectora, protegiéndola de las enzimas en entornos degradantes, como los que se encuentran dentro de los lisosomas. Por lo tanto, la glicosilación es fundamental para la fisiología de las células y los tejidos porque es esencial para el tráfico de proteínas y lípidos a ubicaciones intracelulares apropiadas (figura 1B). Además, al guiar la visualización de lípidos y proteínas clave en las superficies celulares, la glicosilación también es clave para las interacciones entre células. Por ejemplo, las interacciones entre células tisulares e inmunes dan forma a la función de los órganos durante el desarrollo, y la interacción entre las diferentes células inmunitarias que se produce mediante moléculas glicosiladas construye la respuesta inmunitaria. En particular, los autores informan que los glicoARN son ligandos de "siglecs" o receptores de la superficie celular, algunos de los cuales actúan como puntos de control en las células efectoras inmunes.
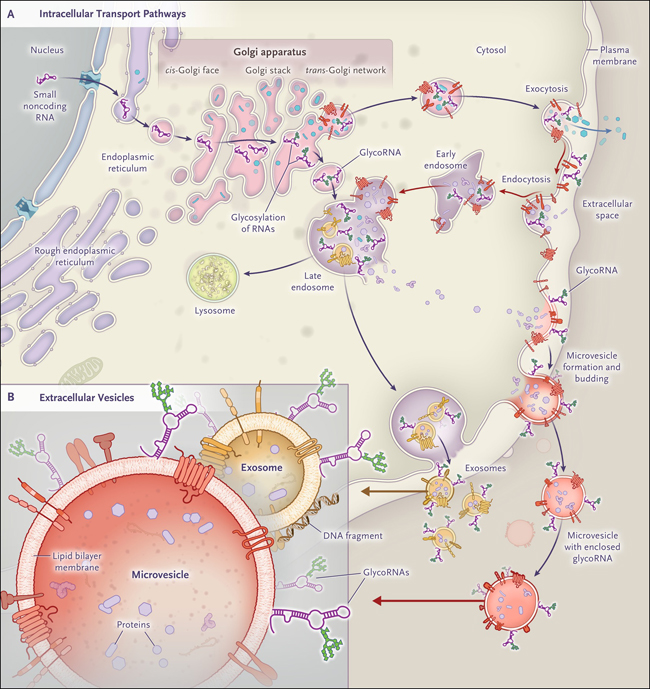
Figura 1: procesamiento y tráfico de glicoARN de superficie celular.
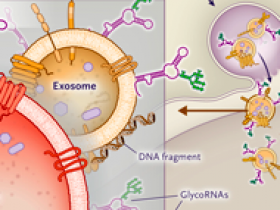
Algunos ARN no codificantes están glicosilados y sialilados y se expresan en la superficie de la membrana plasmática. Además, pueden interactúan con Siglec-15, un inmunosupresor que se regula al alza en las células cancerosas humanas y en las células mieloides que se infiltran en el tumor. La mayoría de los glicoARN celulares se expresan en la superficie celular (panel A), a la que se entregan a través de la vía secretora canónica. Por lo tanto, los glicoARN podrían ser endocitosados y "reciclados" en exosomas que luego se liberan en el medio extracelular tras la fusión de la vesícula "contenedora" con la membrana plasmática. Se ha establecido que algunos exosomas tienen fragmentos de ADN en la superficie. Las microvesículas, que brotan de la membrana plasmática, también pueden transportar glicoARN de superficie (panel B).
Dada la extensa caracterización del sistema secretor y nuestro creciente conocimiento de las modificaciones del ARN, es interesante considerar por qué no se habían encontrado anteriormente glicoARN. Probablemente se deba a suposiciones sobre la biología del ARN y al uso de nuevos métodos experimentales. Los estudios tanto de la glicobiología como de la biología del ARN se han centrado durante mucho tiempo en regiones mutuamente excluyentes dentro de la célula. Si bien el análisis de los glucanos se ha dirigido a la superficie celular, la biología del ARN se ha enfocado principalmente en las regiones nucleares y citoplasmática. Experimentalmente, los glicoARN que se ubican en la superficie celular son particularmente vulnerables a la degradación de la ARNasa, lo que puede explicar por qué habían escapado a la observación anteriormente. El protocolo de extracción y etiquetado metabólico ideado fue clave para el aislamiento de glicoARN.
El descubrimiento de los glicoARN de la superficie celular implica que los ARN, como las proteínas y los lípidos, podrían transportarse a lo largo de la vía secretora. La biogénesis de los glicoARN influiría directamente en la biogénesis de los ARN circulantes, que han estado implicados en trastornos inmunitarios, cáncer, trastornos neurológicos y enfermedades cardiovasculares. Algunos de estos median la comunicación entre células distantes a través de vesículas extracelulares como exosomas y microvesículas que tienen un tamaño aproximado de 50 a 300 nm. Casi todas las células liberan vesículas extracelulares a la circulación y contienen proteínas, fragmentos de ADN y varias clases de ARN, como ARN mensajero, ARN largo no codificante y muchos ARN pequeños no codificantes, incluidos microARN e Y ARN. Sin embargo, la identificación de un mecanismo general que explica cómo se seleccionan los ARN para empaquetarse en vesículas extracelulares del vasto grupo de ARN en el citoplasma ha resultado difícil de dilucidar. La idea de que los ARN, como las proteínas, podrían seleccionarse para su secreción y luego incorporarse en vesículas extracelulares es tentadora. De hecho, la existencia de ARN circulantes y glicoARN de la superficie celular abre un nuevo campo de secreción de ARN.
La perspectiva de la secreción de ARN plantea aún más preguntas. ¿Cómo pueden permanecer anclados a la membrana durante todo el proceso de glicosilación y migración a la superficie celular? ¿Qué sitios del ARN están glicosilados y cuál es la naturaleza del enlace químico entre el ARN y los glucanos? ¿Cómo entrarían los ARN destinados a la glicosilación al retículo endoplásmico en primer lugar? ¿Se seleccionan ARN específicos para su secreción y, de ser así, cuál es el mecanismo? ¿Cuáles son las funciones endógenas de los glicoARN?
De manera más general, ¿cuáles son las ramificaciones clínicas de la presente investigación? El desarrollo de una base molecular y celular sólida para la biogénesis de los ARN circulantes podría fortalecer su utilidad como biomarcadores. Ya existe un sólido precedente para ver los ARN circulantes como marcadores de diagnóstico y pronóstico en el cáncer, y fragmentos de Y ARN, que ahora se han identificado como glicoARN, están alterados en el suero de pacientes con cáncer de mama. Si la expresión de los glicoARN se altera de manera similar en los tumores, pueden representar marcadores de la superficie celular con valor diagnóstico o, alternativamente, un medio para abordar específicamente las células malignas con terapias dirigidas. En el contexto de la enfermedad autoinmune, la biogénesis y la presentación de glicoARN resolvería el hallazgo aparentemente paradójico de que las moléculas intracelulares como el ARN pueden actuar como autoantígenos. Aunque las funciones de los glicoARN en la autoinmunidad y el cáncer son todavía hipotéticas, el descubrimiento de una nueva clase de moléculas abre una nueva frontera de la glicobiología para la investigación biomédica.
Fuente bibliográfica
New Vistas for Cell-Surface GlycoRNAs
Sigrid Nachtergaele, Ph.D., and Yamuna Krishnan, Ph.D.
Department of Molecular, Cellular, and Developmental Biology, Yale University, New Haven, CT (S.N.); and the Department of Chemistry and the Grossman Institute of Neuroscience, Quantitative Biology, and Human Behavior, University of Chicago, Chicago (Y.K.).
N Engl J Med 2021; 385: 658-660