Memoria celular para las heridas
Cuando se producen lesiones de profundidad intermedia, las células madre del folículo piloso migran a la herida y adoptan la función, forma y el patrón de expresión génica de las células madre epidérmicas. Sin embargo, se ha observado que estas células mantienen una memoria epigenética que puede ser clave para mejorar su capacidad regenerativa.
La "memoria" celular, definida como la capacidad distintiva de las células inmunitarias para responder rápidamente a los patógenos, es exhibida por las células de la piel, que, después de la exposición a un estímulo inflamatorio, responden de manera más rápida y robusta cuando se les presenta un segundo estímulo no relacionado. Un reciente informe describe la forma en que las células de la piel codifican múltiples recuerdos de su identidad y experiencias previas. A diferencia de las células inmunitarias, que generan recuerdos al reorganizar permanentemente su ADN, las unidades de la piel producen recuerdos a través de cambios epigenéticos que están asociados con una mayor capacidad de regeneración y curación.
La epidermis y el cabello son generados continuamente por poblaciones de células progenitoras separadas en la base de su epitelio. Los folículos pilosos también contienen una población distinta de células madre, ubicadas en un área llamada protuberancia, que es responsable de producir cíclicamente cabello nuevo. En condiciones homeostáticas, las células progenitoras de la epidermis y del folículo piloso no se mezclan (figura 1, panel superior). Sin embargo, en respuesta a la herida, estas dos poblaciones de células madre se movilizan para cerrar la lesión y formar piel nueva.
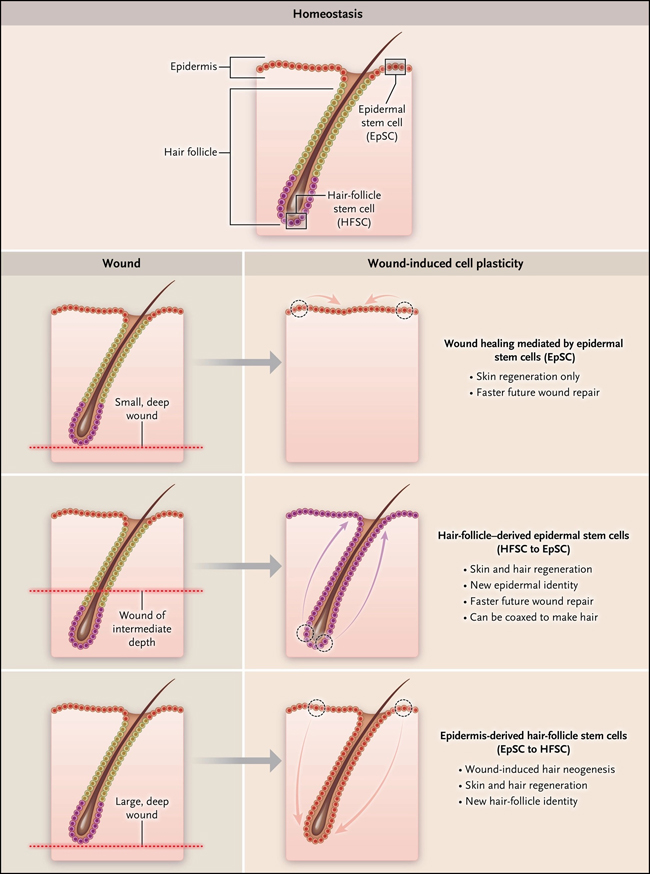
Figure 1: células madre de la piel y plasticidad celular inducida por heridas.
En un modelo de ratón se rastrearon células después de herir a varias profundidades para analizar los tipos de células que curan la piel. Se encontró que las heridas pequeñas y profundas, que resultan en la eliminación del folículo piloso, se repoblaron de células en la epidermis circundante, mientras que las heridas de profundidad intermedia se repoblaron en el folículo piloso (figura 1). La piel curada derivada de células epidérmicas adyacentes no se distinguía de la derivada de células del folículo piloso con respecto a la función y la expresión génica. Las células derivadas del folículo piloso esencialmente asumen una nueva identidad epidérmica, pero un análisis detallado que involucró técnicas moleculares avanzadas descubrió diferencias en la organización de su ADN. En las células madre epidérmicas derivadas de folículos pilosos, áreas específicas de ADN se hicieron más accesibles a través de la cromatina abierta; por lo tanto, el patrón de accesibilidad del ADN dependía del origen celular y de si la célula había respondido a la herida. Por ejemplo, las células que habían respondido previamente tenían regiones de cromatina abiertas que coincidían con genes que se expresan en respuesta a la inflamación y con genes que potencian la migración de células epiteliales durante la cicatrización de heridas (como la subunidad de integrina alfa 5 y el factor de crecimiento de fibroblastos 2). Estas nuevas regiones de cromatina abierta en células madre de la piel previamente lesionadas proporcionaron ventajas funcionales para futuras agresiones (figura 2). Las nuevas heridas en las células madre de la piel previamente heridas indujeron cambios más tempranos en la expresión génica y dieron como resultado una migración celular más rápida que las heridas en las células madre indiferenciadas. En última instancia, las nuevas heridas en la piel previamente dañada se curaron más rápido que las de la piel nueva.
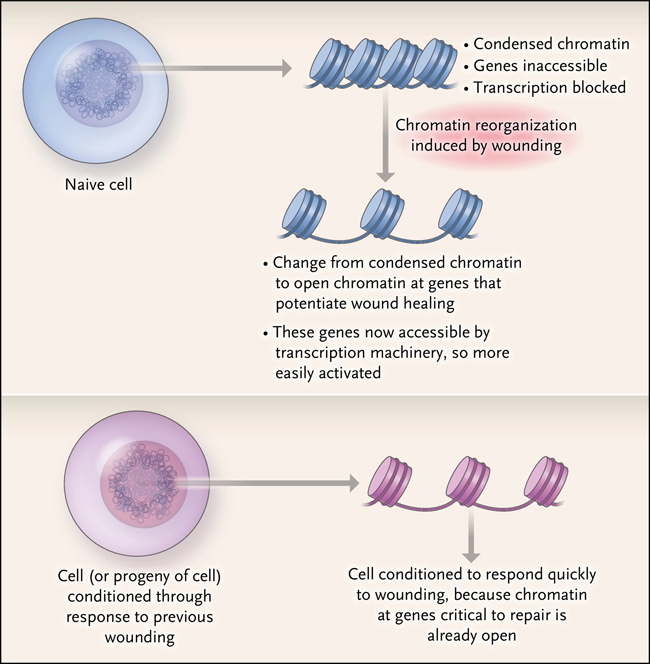
Figura 2: memoria celular epigenética inducida por heridas.
Aunque la conversión de células madre de folículos pilosos en epidermis es importante para la cicatrización, la conversión de células epidérmicas en folículos pilosos introduce la noción de tratar la caída del cabello bajo este enfoque. La neogénesis del cabello inducida por heridas ocurre cuando las células epidérmicas adultas fuera de la protuberancia del folículo piloso migran hacia el centro de la herida y generan nuevos folículos pilosos bajo la influencia de factores secretados por las células inmunitarias y las células dérmicas (figura 1). Aunque no se ha examinado específicamente la neogénesis del cabello inducida por daños, se sabe que la piel derivada de células madre de folículos pilosos tiene más probabilidades de formar folículos pilosos que la piel derivada de células epidérmicas vírgenes cuando se trasplanta a un entorno inductivo. Un fenómeno similar ocurre en las células madre pluripotentes inducidas, que tienden a diferenciarse en su tipo de célula original. Aprovechar esta comprensión puede conducir a tratamientos basados en células para la pérdida de cabello mediante la estimulación de poblaciones celulares específicas con las señales apropiadas.
La observación de que la piel de áreas previamente heridas o inflamadas en ratones está preparada para una curación más rápida brinda una gran oportunidad. Las heridas cutáneas crónicas que no cicatrizan, incluidas las úlceras del pie diabético, las úlceras por presión y las úlceras venosas, son tan frecuentes como la insuficiencia cardíaca, afectando a más de 6 millones de personas al año en los Estados Unidos. Dependiendo del tipo de úlcera, los tratamientos convencionales incluyen desbridamiento quirúrgico, descarga y medias de soporte. Se necesitan urgentemente nuevos tratamientos. Los resultados plantean la posibilidad de pretratar zonas propensas a las úlceras como una manera de crear una "memoria de la herida". Otras investigaciones en animales han demostrado que la crema de imiquimod, que induce inflamación y se usa en la práctica clínica para tratar lesiones precancerosas, puede ser eficaz para cumplir esta función y mejorar la cicatrización. Sin embargo, se necesitan estudios traslacionales y clínicos antes de que estos enfoques puedan considerarse para el manejo experimental de la pérdida de cabello y las heridas crónicas en humanos.
Fuente bibliográfica
Cellular Memories — More Than Skin Deep
Thomas H. Leung and George Cotsarelis
Department of Dermatology, Perelman School of Medicine, University of Pennsylvania (T.H.L., G.C.), and the Corporal Michael J. Crescenz Veterans Affairs Medical Center (T.H.L.).
N Engl J Med 2022; 386:793-795