COVID-19: déficit cognitivo a largo plazo
Un reciente estudio en ratones sobre los efectos neuronales después de una infección leve por SARS-CoV-2 demuestra la presencia de neuroinflamación, identifica un biomarcador candidato y proporciona un marco para estudios posteriores.
Algunos pacientes que se han recuperado de una infección informan de disfunción cognitiva transitoria o incluso duradera. Esto incluye a los que han tenido el SARS-CoV-2, muchos de los cuales, incluidos aquellos con enfermedad leve, padecen deficiencias en la atención, en el funcionamiento ejecutivo, el lenguaje, la velocidad de procesamiento y la memoria, síntomas que en conjunto se denominan “niebla mental”. Junto con una mayor incidencia de ansiedad, depresión, trastornos del sueño y fatiga, este síndrome de deterioro cognitivo contribuye considerablemente a la morbilidad de las condiciones posteriores a COVID-19 (también denominado “COVID prolongado”).
Sin embargo, lo anterior es difícil de diagnosticar y separar de otros síntomas en un paciente individual, porque los datos longitudinales neurocognitivos rara vez están disponibles (no obstante, a nivel poblacional, se ha documentado el deterioro cognitivo posterior). Los médicos generalmente son reacios a aceptar una condición como una enfermedad orgánica sin un concepto patobiológico o la capacidad de medir la enfermedad en un paciente determinado, como es el caso de la niebla mental como secuela. Los resultados de un estudio informado por Fernández-Castañeda y colegas (Cell 2022;185(14):2452-2468.e16) pueden representar un punto de inflexión en nuestra comprensión al respecto.
Utilizando un modelo de ratón, los investigadores exploraron cómo las infecciones respiratorias leves de SARS-CoV-2 podrían conducir a la neuroinflamación y daño cerebral posterior a través de la desregulación de las células neuronales de varios linajes (figura 1). Se modeló una COVID respiratoria leve en un animal que expresaba el receptor de entrada viral para SARS-CoV-2 (enzima convertidora de angiotensina 2 en humanos) en la tráquea y el pulmón al administrarlo por vía intranasal. No lo detectaron en el cerebro, pero encontraron signos de neuroinflamación en niveles elevados de quimiocinas en el líquido cefalorraquídeo y suero, cada uno con un curso distinto de tiempo. Estos cambios condujeron a la activación de la microglía en las regiones de la materia blanca subcortical y del hipocampo (pero no en la materia gris), con efectos diferentes en poblaciones de células neurales específicas. Estos hallazgos fueron respaldados por resultados similares en un pequeño grupo de pacientes que tenían la infección y ningún daño pulmonar grave en el momento de la muerte.
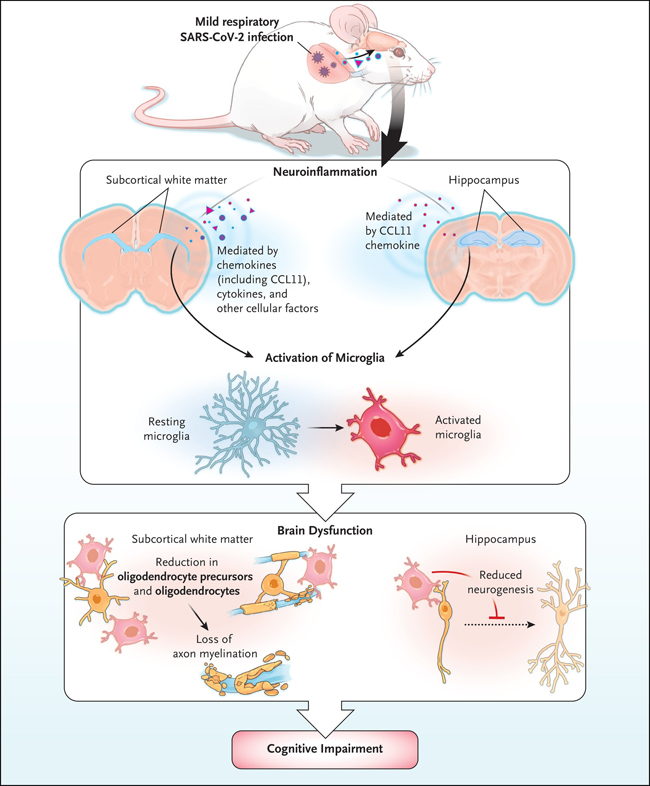
Figura 1: impacto de la infección respiratoria leve por SARS-CoV-2 en las células neurales.
La microglía son células macrófagas residentes en el sistema nervioso central. Aunque contribuyen a la homeostasis del sistema nervioso central y al refinamiento de las redes neuronales al eliminar las espinas dendríticas y las sinapsis durante el desarrollo de las neuronas, la microglía puede pasar a un estado neurotóxico activado, como se ve en este modelo de ratón. En la sustancia blanca subcortical, la activación microglial se asoció con la pérdida de precursores de oligodendrocitos y de oligodendrocitos maduros; consistente con esta merma, también hubo supresión de mielina y axones mielinizados durante al menos 7 semanas después del comienzo de la infección. La mielina aísla los axones y es fundamental para la velocidad de la conducción eléctrica a lo largo de las neuronas y para el metabolismo axonal. La pérdida de axones mielinizados altera la estructura y función de las redes neuronales.
En el hipocampo, la activación de la microglía se asoció con una inhibición de la neurogénesis, lo que podría explicar el deterioro de la formación de la memoria en los pacientes. La activación de la microglía parecía estar mediada por niveles persistentemente elevados de una molécula llamada quimiocina 11 con motivo C-C (CCL11). CCL11 se ha asociado con el envejecimiento y con la inhibición de la neurogénesis. La inyección intraperitoneal sistémica de CCL11 en los animales resultó en la activación de la microglía del hipocampo, pero no de la microglía en la sustancia blanca subcortical. De acuerdo con estos hallazgos, las personas con COVID prolongado y déficits cognitivos tenían niveles más altos de CCL11 en suero que aquellas con COVID prolongado que carecían de síntomas cognitivos. Los pacientes, como los ratones, tenían una enfermedad leve y se infectaron antes de que estuviera disponible la vacuna, pero su número era pequeño (48 con déficit cognitivo y 15 sin).
El efecto de CCL11 en la activación microglial en el hipocampo y la inhibición de la neurogénesis justifica una mayor exploración de los efectos de las quimiocinas y citocinas específicas de los circuitos cerebrales y ofrece potencialmente un marco para estudiar, prevenir y tratar los síntomas neurológicos y psiquiátricos del COVID prolongado. Los hallazgos del equipo de Fernández-Castañeda también tienen paralelos patobiológicos con los síndromes de deterioro cognitivo que han ocurrido después de la terapia oncológica y después de la infección por influenza H1N1 (también se encontró una correlación temporal entre los niveles elevados de quimiocinas y citocinas y el deterioro de la neurogénesis del hipocampo después de la infección por H1N1 en ratones).
¿Podrían estos resultados conducir a una cura para la niebla mental relacionada con COVID? Se han evaluado varios fármacos dirigidos a la microglía activada en modelos preclínicos de síndromes de deterioro cognitivo mecánicamente similares. El pexidartinib, un inhibidor del receptor CSF1, ha sido aprobado por la FDA para el tratamiento de tumores tenosinoviales de células gigantes sintomáticos, pudiendo agotar la microglía. Ciertos agentes antiinflamatorios no esteroideos y tetraciclinas son capaces de inhibir la microglía. Todo lo anterior respalda a los moduladores microgliales para tratar la niebla cerebral relacionada con COVID.
El estudio también implica a CCL11 como biomarcador candidato. Si este hallazgo se valida a través de una investigación, sus niveles en el plasma o líquido cefalorraquídeo podrían identificar potencialmente a pacientes con deterioro cognitivo relacionado a COVID. Los ensayos también se utilizaríab para analizar el efecto de las vacunas en los cambios relacionados con la niebla cerebral. Sin embargo, debido a que solo se estudiaron pequeñas cohortes de pacientes y factores como el sexo y el historial de enfermedad autoinmune pueden influir en las concentraciones séricas de CCL11, se requieren estudios clínicos en cohortes grandes para excluir las variables de confusión y corroborar aún más a CCL11 como biomarcador. La especificidad puede aumentar cuando se incluyen otros perfiles de citoquinas o quimioquinas o con un enfoque más limitado en los niveles de CCL11 en el líquido cefalorraquídeo, ya que existe una superposición sustancial de los niveles séricos de CCL11 en individuos con niebla cerebral y en aquellos que no la tienen.
El hallazgo de desmielinización axonal (o mielinización alterada) en secciones de cerebro de ratón podría inspirar el desarrollo de nuevos biomarcadores de imágenes por resonancia magnética para humanos. Sin embargo, aquí se consideró la cepa más antigua de SARS-CoV-2 (Wuhan-Hu-1 o USA-WA1/2020); la relevancia de estos hallazgos para la niebla cerebral asociada con la infección por otras variantes del SARS-CoV-2 parece probable pero incierta. Además, como señalan los propios autores, la contribución de otros tipos de células, como los astrocitos, a la confusión mental relacionada con la COVID-19 puede ser considerable. Finalmente, existe la advertencia habitual de que los ratones no son humanos, por lo que se justifican pruebas sólidas de replicación en estudios que involucren a un mayor número de pacientes. Aunque los resultados de la disfunción cerebral y los patrones de daño durante y después de la COVID son preocupantes, especialmente dadas las similitudes con los cambios en las enfermedades neurodegenerativas humanas, los estudios traslacionales como estos pueden solventar diagnósticos y tratamientos precisos.
Fuente bibliográfica
Cognitive Deficits in Long Covid-19
Varun Venkataramani y Frank Winkler
Department of Neurology, University Hospital Heidelberg, Heidelberg, Germany.
N Engl J Med 2022; 387:1813-1815